The Korea-EU FTA must be dismantled. And the lives of patients in over 120 countries are on the line regarding the India-EU FTA. What will devastate the Pharmacy of the World must also be stopped.
오는 3월 2일에 전 세계의 민중들의 생명을 담보로 하는 인도-EU FTA협상중단을 촉구하는 국제공동투쟁을 벌일 것입니다. 한국에서도 3월 2일에 한EU, 인도EU FTA폐기를 촉구하는 기자회견을 갖고자 합니다.
현재까지 신종 인플루엔자(H1N1·이하 신종 플루)의 보편적인 치료제는 스위스계 제약회사 로슈가 생산·판매를 독점하는 오셀타미비르(Oseltamivir), 즉 ‘타미플루’(Tamiflu)다. 2004년 과학전문지 는 백신이 광범위하게 보급되기 전까지, 혹은 그 이후에도 타미플루가 인플루엔자의 대유행에 맞서는 유일의 방어책이라고 평가하기도 했다. 그러나 그때도 그랬고 지금에 와서는 더욱 분명해진 문제점은 세계적 대유행과 같은 비상시에 사용할 수 있는 치료제의 비축분이 부족하다는 사실이다. 개발도상국과 제3세계 국가에서는 특히 그러하다.
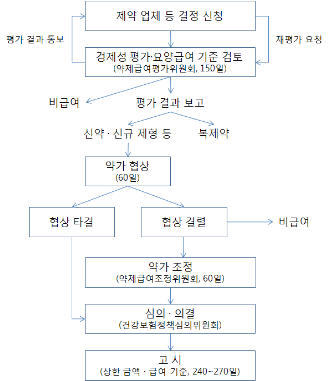
한국의 의약품 지출 경향의 특징을 살펴보기 위해서는 국민건강보험 총 진료비 중 약제비 비중을 살펴보면 된다. 약제비 지출 비중은 2001년 23.5%에서 2006년 29.4%로 증가하였고(OECD평균 17.8%차지, 2003년), 2001년 이후 5년간 약제비 증가율도 연평균 15.0%로 동일기간 진료비 증가율 10.6%에 비하여 증가속도가 매우 급속하게 나타났다1. 또한, 사회보험을 가지고 있는 국가이면서도 약제비에 대한 사적 지출의 비중이 약 48%로 높다2. 우리나라는 이러한 약제비 증가에 대한 대응으로써 2006년 12월부터 약제비적정화방안을 시행하고 있다.
<조승수 의원실 정책보고서> 특허 발명의 정부 사용 제도 개선방안 – 국제조약과 해외 입법례 검토 –
조승수 의원은 오는 11월 12일(목) 오전10시 국회의원회관 128호에서는, 조승수 의원이 대표발의한 『특허법 법률 개정안』(106조 개정안, 특허 발명의 정부 사용제도)에 대한 토론회를 개최한다. (토론회 기획안 참고)
지난 5월 7일, 보건복지가족부에서 백혈병치료제 스프라이셀(sprycel)의 가격을 결정하기 위해 네 번째 약제급여조정위원회가 열렸다. 2008년 1월 14일, 국민건강보험공단과 스프라이셀을 생산하는 다국적 제약회사 BMS(Bristol-Myers Squibb) 간의 협상이 결렬됐다. 그리고 3월 14일 첫 번째 조정위원회가 열린 이후 이미 2달 가까이 지난 이 날, 스프라이셀의 약값은 한 캅셀에 55,000원이라는 경이로운 가격으로 결정됐다. 성인 하루 복용량이 두 캅셀이니, 백혈병 환자들은 하루에 11만원, 1년이면 약 4천여만 원에 달하는 약값을 감당해야 한다. 조정위원회의 이성환 위원장은 이 날 기자들과의 인터뷰에서 55,000원은 “제약회사가 공급을 거부하지 않을 최선의 선택”이라고 이야기 했다.
제네릭 의약품과 자료독점권(Data Exclusivity) 제네릭의약품은 오리지널의약품과 대별되어 사용되기도 하고, 특허의약품과 대별되어 사용되기도 한다. 전자는 의약품판매허가와 관련이 있는데, 오리지널의약품의 ‘활성성분(active ingredient)’과 동일한 화합물을 포함하여 오리지널의약품과 같은 효과를 가지는 의약품을 의미하고, 후자는 특허받은 의약품과 실질적으로 동일한 발명으로 보이는 의약품을 통상 일컫는 말이다. 의약품의 판매허가제도와 특허제도는 분명 다른 것이나 제네릭의약품이 두 제도에 모두 연관되어 사용되는 이유는 이 두 제도가 의약품의 독점을 보장하고 있기 때문이다. 즉 의약품 판매허가제도와 특허제도에서 통용되는 제네릭의약품은 두 제도가 보장하는 독점에 의해 더 이상 보호받지 않고 첫 번째 제약회사(오리지널의약품 제조회사 혹은 특허의약품 제조회사)외의 다른 회사에 의해 복제 혹은 생산될 수 있는 의약품을 의미한다. 그러나 판매허가기준과 특허기준이 다르기 때문에 두 제도에서 기인하는 제네릭의약품의 대상과 범위는 다를 수 있다.
